국내 연구진이 세균의 강력한 미생물막인 '바이오필름(biofilm)'을 무력화시키는 플랫폼을 개발해 주목됩니다. 인체 다제내성균인 '슈퍼박테리아' 문제를 해결할 목적으로 개발되었지만, 축산에서도 활용 가능성이 있습니다.
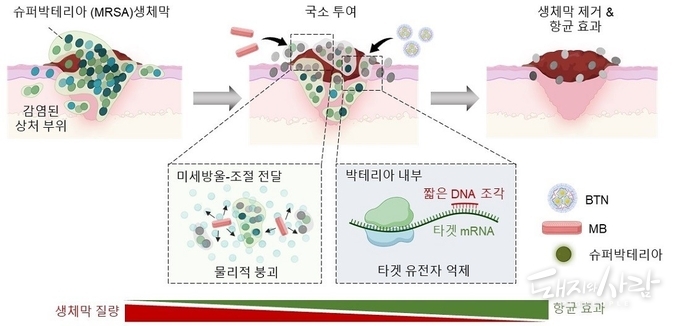
카이스트(KAIST) 생명과학과 정현정 교수 연구팀은 미국 일리노이대 공현준 교수팀과의 공동연구를 통해, 포도상구균이 형성한 세균성 바이오필름을 효과적으로 제거하기 위해 유전자 억제제를 세균 내부로 정확하게 전달하는 미세방울 기반 나노-유전자 전달 플랫폼(BTN‑MB)를 개발했다고 29일 밝혔습니다.
연구팀은 먼저, 포도상구균의 주요 유전자 3종 ▶바이오필름 형성(icaA) ▶세포 분열(ftsZ) ▶항생제 내성(mecA)을 동시에 억제하는 짧은 DNA 조각(oligonucleotide)을 설계하고, 이를 탑재해 균내로 효과적으로 전달할 수 있는 나노입자(BTN)를 고안했습니다.
여기에 더해, 미세방울(microbubble, 이하 MB)을 사용해 포도상구균이 형성한 바이오필름인 미생물막의 투과성을 높이도록 했습니다. 연구팀은 이 두 가지 기술을 병용해, 세균의 증식과 내성 획득을 원천적으로 차단하는 이중 타격 전략을 구현했습니다.
이 치료 시스템은 두 단계로 작동합니다. 먼저, 미세방울(MB)이 포도상구균이 형성한 세균성 생체막내 압력 변화로 나노입자의 침투를 가능하게 만듭니다. 이어, 나노입자가 생체막의 틈을 타 세균 내부로 침투해 유전자 억제제를 정확하게 전달합니다. 이를 통해 포도상구균의 유전자 조절을 일으켜 생체막 재형성, 세포 증식, 그리고 항생제 내성 발현이 동시에 차단됩니다.

실제 돼지 피부 감염 생체막 모델과 포도상구균 감염 마우스 상처 모델에서 시행한 실험 결과, BTN‑MB 치료군은 생체막 두께가 크게 감소했으며, 세균 수와 염증 반응도 현저히 줄어드는 뛰어난 치료 효과를 확인할 수 있었습니다.
이러한 결과는 기존 항생제 단독 치료로는 달성하기 어려운 수준이며, 향후 다양한 내성균 감염 치료에도 적용할 수 있는 가능성을 보여줍니다.
연구를 주도한 정현정 교수는 “이번 연구는 기존 항생제로는 해결할 수 없는 슈퍼박테리아 감염에 대해 나노기술, 유전자 억제, 물리적 접근법을 융합해 새로운 치료 해법을 제시한 것”이라며, “향후 전신 적용 및 다양한 감염 질환으로의 확장을 목표로 연구를 지속할 것”이라고 설명했습니다.
이번 연구 논문은 지난 19일 국제학술지(Advanced Functional Materials)에 온라인 게재됐습니다(바로가기).
이득흔 기자(pigpeople100@gmail.com)